
世界の残留DNA検査市場の 洞察:2034年までの予測
- 世界の残留DNA検査市場規模は、2024年に2億6000万米ドルと評価されました
- 市場規模は2024年から2035年にかけて6.5%のCAGRで成長しています
- 世界の残留DNA検査市場規模は、2035年までに5億2000万米ドルに達すると予想されています
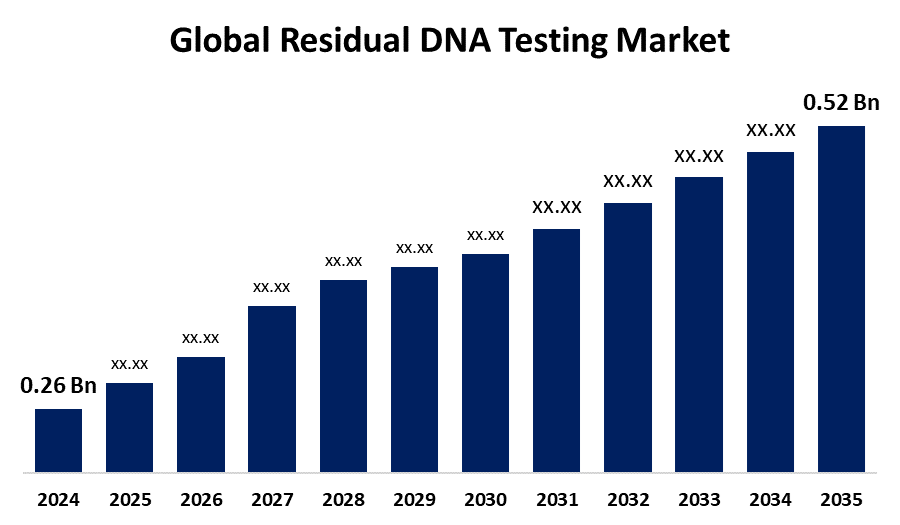
世界の残留DNA検査市場規模は、2024年の2億6000万米ドルから2035年までに5億2000万米ドルに成長し、2025年から2035年の予測期間中に6.5%のCAGRで成長すると予想されています。
市場概況 -
世界の残留DNA検査市場は、バイオ医薬品の製造やワクチン開発における品質管理に対する需要の高まりにより、着実に成長しています。残留DNA検査は、生物製剤の製造中に残された微量の宿主細胞DNAが、安全で許容範囲内にあることを確認します。規制当局は、DNA残留レベルに関する厳格なガイドラインを義務付けており、高度な試験方法の採用を推進しています。市場は、バイオ医薬品とバイオシミラーの台頭、分析技術の技術的進歩、医薬品製造における製品の安全性と規制遵守への注目の高まりによってさらに支えられています。
推進要因
世界の残留DNA検査市場の成長は、厳格な品質管理を必要とするバイオ医薬品やバイオシミラーの生産の増加など、いくつかの重要な要因によって推進されています。製品の安全性を確保し、汚染リスクを最小限に抑えるようにという保健当局からの規制当局からの圧力により、残留DNA検査が広く採用されるようになりました。分子生物学や、qPCRや次世代シーケンシングなどの分析試験における技術的進歩も、より迅速で正確な検出を支えています。さらに、ワクチンや細胞治療の開発における安全性への注目の高まりは、信頼性の高いDNA残留物検査ソリューションの需要をさらに高めています。
抑制要因
世界の残留DNA検査市場は、高度な検査技術や機器の高コストなど、いくつかの抑制要因に直面しており、特に小規模なバイオ医薬品企業の間で採用が制限される可能性があります。さらに、テスト手順の複雑さと熟練した人員の必要性は、運用上の課題を引き起こす可能性があります。また、地域間で規制ガイドラインが異なるため、試験基準に一貫性が生じず、グローバルなコンプライアンスがさらに複雑になる可能性があります。これらの要因は、新興市場での認知度が限られていることと相まって、市場の全体的な成長を妨げる可能性があります。
残留DNA検査市場は、主に生物製剤とバイオシミラーの規制当局承認数の増加に牽引されて、大幅な成長を遂げています。規制当局からの厳格なガイドラインにより、これらの製品の安全性と有効性を確保するために、残留DNAアッセイの必要性が高まっています。さらに、新興市場は、研究開発投資の増加に支えられて新たな成長機会を生み出しており、これにより主要なプレーヤーの市場の範囲と競争力が拡大しています。
テストタイプ別 2024年、最終製品のリリーステストは、残留DNAテスト市場で最大のシェアを占めました。
このセグメントは、原材料試験、バルクロット放出試験、最終製品出荷試験を含む広範な分類の一部です。最終製品リリーステストの優位性が高まっているのは、最終製造段階での正確なプロセス最適化と信頼性の高いバッチリリース保証の必要性によるものです。この時点で、精製プロセスを強化し、最終製品中の残留DNA含有量を最小限に抑えるためには、残留DNA検査の実施が不可欠です。これらのアッセイは、精製ステップの検証だけでなく、厳しい規制基準への準拠を実証するためにも重要です。
エンドユーザー別(製品)製薬およびバイオテクノロジー企業は、2024年に最も急成長し、最大のエンドユーザーセグメントでした。
この成長の主な要因には、高度な治療法や生物学的製剤開発への投資の増加などがあります。さらに、臨床検査および臨床検査サービスのアウトソーシングへの強い傾向により、残留DNA検査製品の需要が加速しています。規制コンプライアンスは引き続き主要な推進力であり、企業は厳格な品質と安全性のベンチマークを満たす必要があります。
地域別では、2024年に北米が残留DNA検査市場をリードしました。
専門メーカーとサービスプロバイダーの強力な存在感によるものです。特に米国では、急速に拡大するバイオ医薬品セクターからの需要が急増しています。この成長は、規制当局と生物製剤研究に関与する組織との間の戦略的協力によって支えられています。例えば、American Type Culture Collection(ATCC)とU.S. Pharmacopeia(USP)のパートナーシップのようなパートナーシップにより、ゲノムDNA分析標準物質(ARM)が誕生しました。これらのARMは、生物学的製剤中の残留DNAを正確に測定するために重要であり、品質管理環境での使用をガイドする詳細なアプリケーションノートが付属しています。
キープレーヤー
- バイオ・ラッド研究所
- 富士フイルム株式会社
- キアゲン
- チャールズリバー研究所
- メルク KGaA
- サーモフィッシャーサイエンティフィック(株)
- マラバイライフサイエンス
- ユーロフィン・サイエンティフィック
市場セグメント
世界の残留DNA検査市場、製品・サービス
- 消耗 品
- 機器およびソフトウェア
世界の残留DNA検査市場、技術
- PCR検査
世界の残留DNA検査市場、検査タイプ
- 原材料試験
- 最終製品リリーステスト
- バルクロットリリース試験
世界の残留DNA検査市場、アプリケーション
- モノクローナル抗体 (mAb)
- 細胞・遺伝子治療(CGT)
- ワクチン
世界の残留DNA検査市場、エンドユーザー
- 製薬・バイオテクノロジー関連企業
- CROおよびCDMO
世界の残留DNA検査市場、 地域分析
- 北アメリカ
- 私達
- カナダ
- メキシコ
- ヨーロッパ
- ドイツ
- 英国
- フランス
- イタリア
- スペイン
- ロシア
- その他のヨーロッパ諸国
- アジア太平洋
- 中国
- 日本
- インド
- 大韓民国
- オーストラリア
- その他のアジア太平洋地域
- 南アメリカ
- ブラジル
- アルゼンチン
- 南アメリカの他の地域
- 中東・アフリカ
- アラブ首長国連邦
- サウジアラビア
完全な目次(Table of Contents)をリクエスト
以下の情報をご入力いただくと、完全な目次をお送りいたします。
ライセンスを確認
シングルユーザー、マルチユーザー、エンタープライズなど、 お客様のニーズに最適なプランをお選びください。
当社の市場調査内容
- 24時間365日 アナリストサポート
- 世界各国のクライアント
- カスタマイズされたインサイト
- 技術進化の分析
- 競争インテリジェンス
- カスタムリサーチ
- シンジケート市場調査
- 市場スナップショット
- 市場セグメンテーション
- 成長動向
- 市場機会
- 規制動向の概要
- イノベーションと持続可能性
